全球首个口服抗新冠病毒药物获批,可治疗中轻度新冠患者(组图)
刚刚,抗新冠病毒药物Molnupiravir(EIDD-2801/MK-4482),获得了英国药品和保健产品监管局(MHRA)的上市批准,用于治疗轻度到中度新冠肺炎患者。
这意味着人类终于有了第一个对抗新冠病毒的口服药物。
英国MHRA的这次审批是基于3期临床试验(MOVe-OUT)的中期分析结果。
从研究结果来看,在高危、不需要住院的轻度到中度新冠肺炎患者(体内至少有一种风险因子预示其可能发展成危重症)中,与对照组相比,口服Molnupiravir将患者住院或死亡风险降低约50%,死亡风险降低100%[1]。
由于试验数据过于优秀,在与美国FDA协商后,这个研究的招募工作被提前终止。
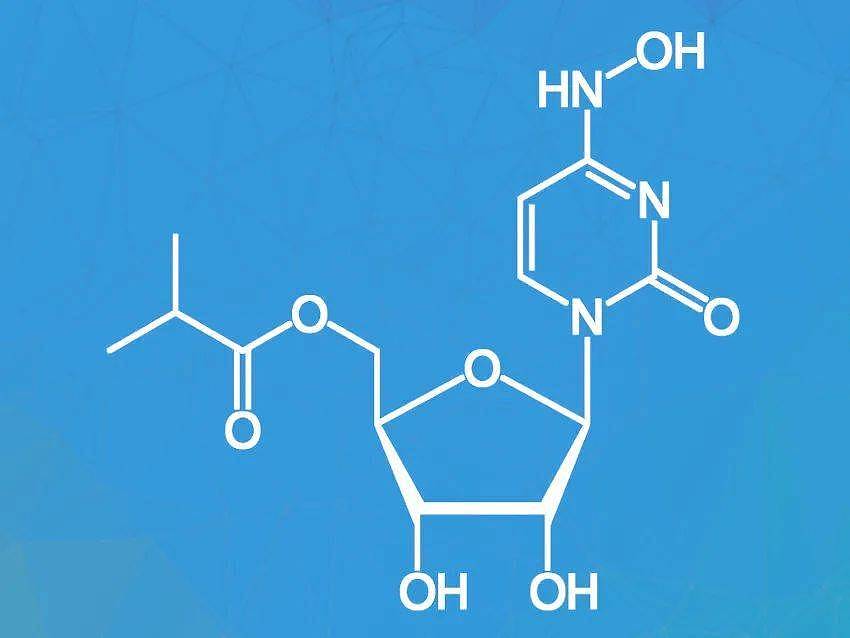
Molnupiravir化学式
估计很多人都不知道,全球累计新冠肺炎确诊病例已经超过2亿了。
新冠疫苗的诞生,在一定程度上遏制了新冠肺炎在全球的蔓延,让无数人免于感染新冠病毒以及因感染而死亡。然而抗新冠病毒的药物的研发一直滞后。
时至今日,获得美国FDA批准上市的抗新冠病毒药物,只有用于治疗重症住院新冠感染者的瑞德西韦。
不过,瑞德西韦的疗效有限,3期临床研究ACTT-1的最终结果显示:接受瑞德西韦治疗的患者中位恢复时间缩短了5天[2]。值得一提的是,在第29天时,基线时需要吸入低通量氧气的患者获益更大,安慰剂组的死亡率是13%,而瑞德西韦组是4%(HR,0.30)[2]。
很多研究人员认为,对付新冠病毒要“早下手,下重手”。因为随着患者的病情加重,治疗难度变大,药物的疗效也变差。因此,开发对早期感染有效、价格低廉、且可及性强的药物,显得尤为重要。
实际上,在新冠疫情爆发早期,科学家就马不停蹄地在筛选任何有可能对抗新冠病毒的药物。
新冠病毒
Molnupiravir就是科学家努力的产物。
Molnupiravir最初是由埃默里大学全资拥有的非营利性生物技术公司Drug Innovations at Emory (DRIVE)开发的,目的是治疗由蚊子传播的委内瑞拉马脑炎病毒感染。
2015年的时候,DRIVE的首席执行官George Painter将Molnupiravir提供给范德堡大学的病毒学家Mark Denison,测试Molnupiravir抗冠状病毒的效果。结果Molnupiravir表现不俗,对SARS和MERS等多种冠状病毒都有较强的抑制效果[3]。
新冠疫情爆发之后,DRIVE将Molnupiravir授权给制药公司Ridgeback Biotherapeutics,由Ridgeback Biotherapeutics和默沙东联合开发。
就在去年,研究人员在雪貂身上的研究表明,Molnupiravir不仅能抑制新冠病毒的复制能力,还能抑制病毒从受感染的雪貂向未受感染的雪貂传播[4]。
几乎在同一时期启动的3期临床试验MOVe-OUT,也在今年的10月1日发布了前文提到的中期分析数据。
具体来看,在接受治疗29天后,在Molnupiravir组有7.3%的患者住院(28/385),没有患者死亡;而安慰剂组有14.1%的患者住院或死亡(53/377),其中患者8名死亡[1]。
更厉害的是,从分析结果来看,Molnupiravir对Delta变种、Gamma变种和Mu变种等新冠变种表现出了一致的疗效。
从不良事件发生率来看,Molnupiravir组和安慰剂组的任何不良事件发生率分别为35%和40%,药物相关不良事件的比例分别为12%和11%,因不良事件而停止治疗的比例分别为1.3%和3.4%[1]。
总的来看,对于高危、不需要住院的轻度到中度新冠肺炎患者而言,Molnupiravir安全有效。
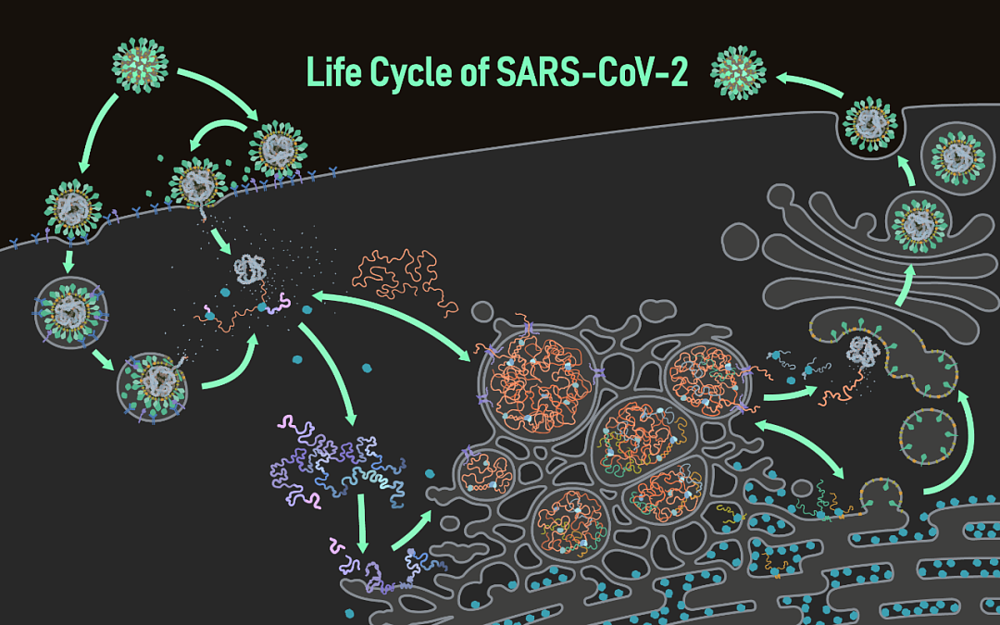
新冠病毒的生命周期
Molnupiravir与瑞德西韦一样,都属于核苷酸类似物。因此,它们都有机会插入到新冠病毒的RNA中去。
尽管是同一类药物,Molnupiravir与瑞德西韦的抗病毒机制并不相同。
之前有研究表明,瑞德西韦主要与ATP竞争[5]。也就是说,在RNA的合成过程中,RNA依赖的RNA聚合酶(RdRp)会在原本该加入ATP的地方,加入瑞德西韦,瑞德西韦直接卡在RdRp和模版RNA之间,导致RNA的合成终止,病毒的复制随之终结。
简单地说,新冠病毒是被瑞德西韦“卡死”了。
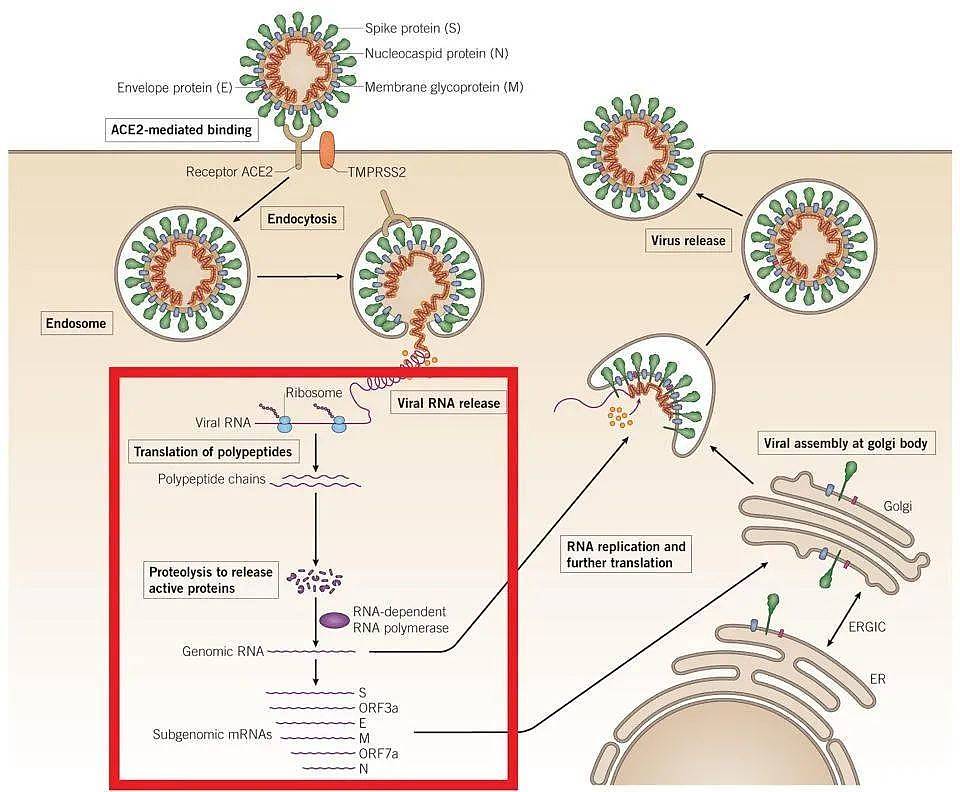
核苷酸类似物前体药物的作用阶段
而Molnupiravir则不一样,它的作用机制与瑞德西韦相比至少有两大不同。
第一处不同是,Molnupiravir的结构非常灵活,它不仅能模拟CTP,还能模拟UTP,也就是说Molnupiravir会同时与CTP和UTP竞争,随机插入到新冠病毒的RNA中[6,7]。
虽然Molnupiravir也会插入到新冠病毒的RNA之中,但是Molnupiravir不会“卡死”RdRp,而是让RdRp完成新冠病毒RNA的合成[6,7]。这就是第二个不同之处。
乍一看Molnupiravir好像没能抑制新冠病毒的复制。实际上,新冠病毒崩溃的伏笔已经埋下了。
要知道,无论Molnupiravir插到RNA的何处,它都是一个点突变。当Molnupiravir插入的足够多之时,新冠病毒就崩溃而亡了。
对于这种抗病毒机制,研究人员称其为“致命诱变”。
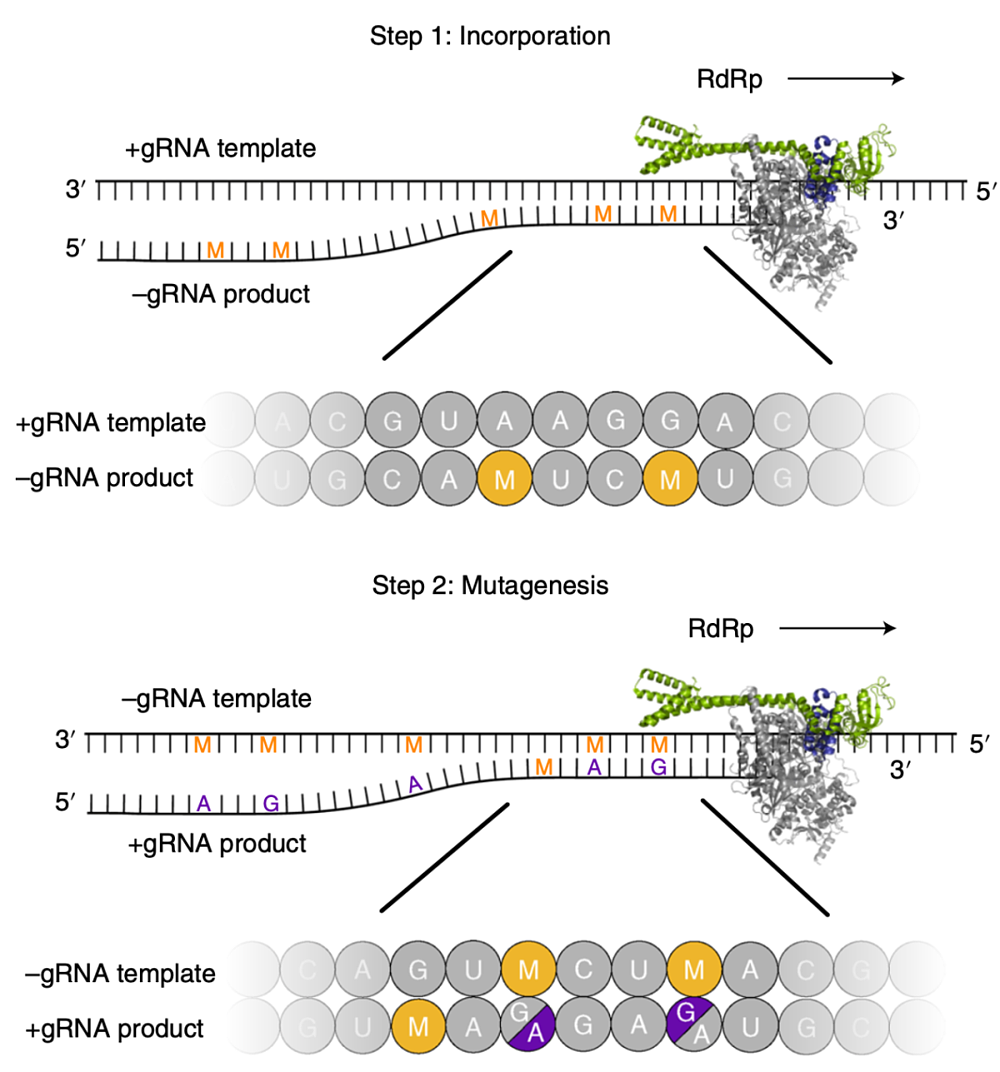
致命诱变的过程
值得一提的是,由于Molnupiravir导致的突变是随机的,新冠病毒很难对这种抗病毒方式产生耐药性,临床前的基础研究也证实了这一点[6,7]。
这种“致命诱变”的抗病毒方式,也让一些研究人员有所担心,怕它会影响DNA的合成,带来一些安全问题。由于目前还没有相关的安全性数据发布,我们还不确定这种担心是否有必要。不过,默沙东的首席科学官Daria Hazuda认为,只要按计划用药,这个药物它就是安全的。
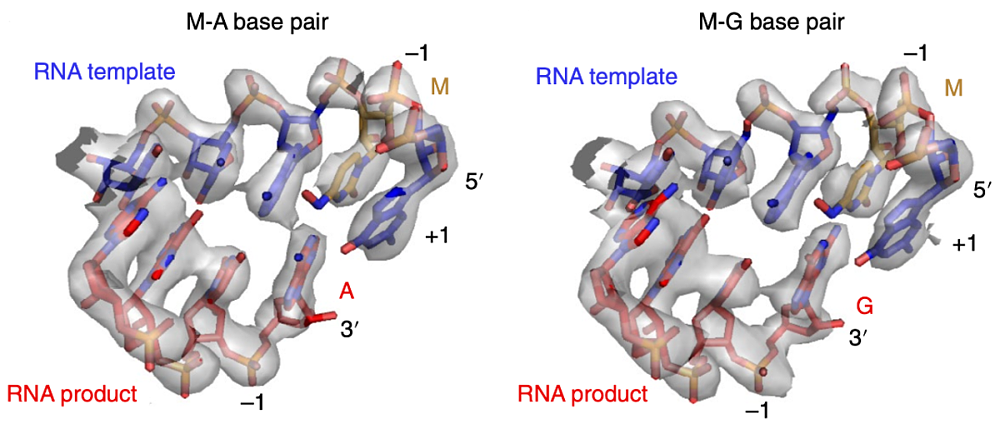
插入后的配对
那么Molnupiravir有没有可能遏制新冠疫情的发展呢?
在研究人员看来,至少有两个关键问题要解决[8]。
第一,从目前的研究数据来看,新冠感染者需要在感染早期使用Molnupiravir,这对于很多诊断能力不足的国家而言,非常有挑战性。
第二,Molnupiravir的价格并不便宜。据了解,美国政府已经同意以12亿美元的价格购买170万个疗程的Molnupiravir,这样算来,一个疗程的费用超过700美元。虽然比瑞德西韦和抗体便宜了很多,但是对大部分国家来说,这个价格还是太贵了。好在制药企业正在寻求解决的办法。
总的来说,即使抗新冠病毒的特效药真的出现了,还是得靠全世界各个国家通力合作,只有全球都实现早诊早治,才能真正遏制新冠疫情的蔓延。
毕竟在全球性疫情面前,人类是一个命运共同体。









 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


